12月6日,同济大学附属第十人民医院彭文辉教授团队在《自然·通讯》(Nature Communications)在线发表了题为“Extracellular traps from activated vascular smooth muscle cells drive the progression of atherosclerosis”的研究论文。该研究首次揭示了在动脉粥样硬化斑块进展过程中,血管平滑肌细胞发生巨噬细胞转分化伴随PAD4表达升高,发生细胞外捕捉这一生物学现象。细胞外捕捉释放的DNA等物质,通过激活斑块中其他细胞的TLR4信号通路和STING-SOCS1信号通路,加速血管平滑肌细胞向致病性转分化,促进斑块进展和不稳定。该研究结论为动脉粥样硬化中血管平滑肌细胞命运重编程后相关功能研究填补了空白,为精准化靶向干预血管平滑肌细胞转分化方向从而治疗动脉粥样硬化疾病提供了理论依据。

细胞外捕捉现象最初发现在中性粒细胞受到微生物感染后,这一系列的特殊细胞现象包括蛋白瓜氨酸化、染色质解聚、颗粒蛋白释放,形成的网状结构对外源性微生物包绕、捕捉,并将外源微生物杀死。近年来,细胞外捕捉被发现也参与到非感染性疾病、自身免疫性疾病等无菌性炎症中,而且除中性粒细胞外,巨噬细胞等免疫细胞也可以产生细胞外捕捉。但目前对于细胞外捕捉在动脉粥样硬化中的研究显示其可影响动脉粥样硬化,但并非依赖中性粒细胞来源的途径,所以是否存在其他细胞来源的细胞外捕捉还是研究空白。
该研究采用血管平滑肌细胞谱系示踪小鼠(Myh11-cre/ERT2/B6/JGpt-H11em1Cin(CAG-LoxP-ZsGreen-Stop-LoxP-tdTomato)/Gp,简称 Myh11Cre/B6G)结合PCSK9-AAV鼠尾静脉注射联合高脂饲料喂养进行动脉粥样硬化疾病造模,首次证明在晚期斑块中,血管平滑肌细胞转分化而来的巨噬细胞是细胞外捕捉的重要来源(图1)。
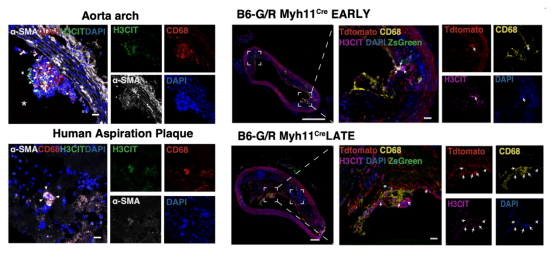
图1:巨噬细胞特别是平滑肌细胞来源的巨噬细胞是晚期斑块中细胞外捕捉的重要来源
为了进一步明确血管平滑肌细胞来源巨噬细胞外捕捉对斑块进展的影响,研究者构建了三基因敲除小鼠(Myh11Cre/B6G/Pad4flox/flox)并制成动脉粥样硬化模型,通过流式分选Tdtomato+的血管平滑肌细胞结合单细胞测序技术,首次探讨了体内抑制血管平滑肌细胞产生细胞外捕捉通过改变血管平滑肌细胞命运重编程方向,从而影响动脉粥样硬化不稳定性和斑块进展。进一步提示了血管平滑肌细胞来源巨噬细胞产生细胞外捕捉对于改变斑块内微环境具有重要作用(图2)。
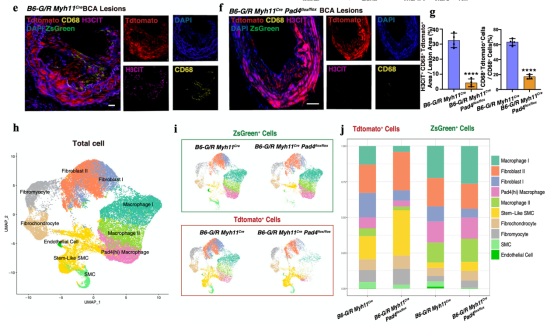
图2:血管平滑肌细胞来源的巨噬细胞产生细胞外捕捉可通过影响血管平滑肌细胞转分化方向促进斑块进展和加重斑块不稳定
综上所述,本研究发现血管平滑肌细胞转分化为巨噬细胞后,通过释放细胞外捕捉激活周围血管平滑肌细胞,促进血管平滑肌细胞向巨噬细胞样等有害型细胞转分化。细胞外捕捉在动脉粥样硬化斑块微环境中激活周围血管平滑肌细胞衍生细胞的STING-SOCS1信号通路和TLR4-MYD88信号通路,抑制STAT3磷酸化过程,促进血管平滑肌细胞向有害细胞转分化,并促进MMP9、MMP12和TNF-α的释放,加速胶纤维降解,促进斑块进展和不稳定斑块的形成(图3)。该研究围绕血管平滑肌细胞转分化为巨噬细胞后产生细胞外捕捉这一新型生物学现象,提出了精准靶向血管平滑肌细胞转分化方向作为抗动脉粥样硬化斑块进展的新型治疗靶点和研究思路。
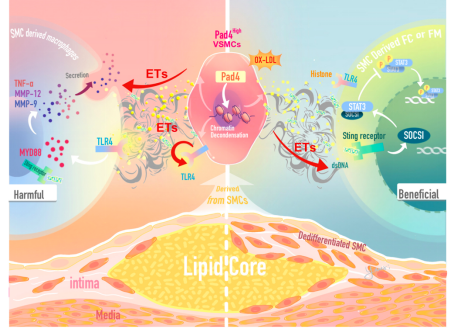
图3:血管平滑肌细胞来源的巨噬细胞通过细胞外捕捉影响斑块进展和稳定度
同济大学附属第十人民医院彭文辉教授为论文唯一通讯作者,同济大学翟鸣、贡时雨博士研究生为论文共同第一作者。
论文链接:https://www.nature.com/articles/s41467-022-35330-1
