10月5日,同济大学附属第一妇婴保健院、生命科学与技术学院毛志勇教授团队与同济大学生命科学与技术学院、附属东方医院孙方霖教授团队联合在PNAS(《美国科学院院报》)上在线发表了题为“Rational combination therapy for hepatocellular carcinoma with PARP1 and DNA-PK inhibitors”的研究工作。该研究首次利用小鼠报告模型在体内比较了肝细胞癌和癌旁组织的DSB修复能力,发现肝细胞癌中同源重组(Homologous recombination, HR) 和非同源末端连接(Nonhomologous end joining, NHEJ)修复效率均显著上调,而PARP1 和 DNA-PKcs是介导该变化的关键基因。进一步的研究提示,同时靶向抑制 PARP1 和 DNA-PKcs 酶活显著抑制了小鼠原位肝细胞癌和人肝细胞癌的PDX模型的增殖,提示其具有重要的潜在临床应用价值。

全球每年有近60万人因肝癌死亡,在所有癌症的死亡人数中排名第二。而由于乙肝流行等因素,中国成为世界范围内的肝癌高发地区,肝癌发病率约为欧美国家的4倍。在所有不同类型肝癌中,肝细胞癌(hepatocellular carcinoma, HCC)最为常见。由于缺少有效的分子靶向治疗手段,肝细胞癌的致死率依然居高不下,5年生存率仅为10%。因此,深入阐述肝细胞癌发生发展的分子机制,并基于此寻找新的更高效安全的分子靶点以治疗肝细胞癌迫在眉睫。
DNA双链断裂(DNA double strand breaks, DSBs)是对机体危害最大的DNA损伤类型,这种损伤由独立且互相竞争的同源重组 (HR)和非同源末端连接(NHEJ)来修复,以维持基因组的稳定性。DNA修复能力下降引发的基因组不稳定现象是包括肝癌在内的多种肿瘤发生的重要诱因;而另一方面,肿瘤细胞却需要激活自身DNA修复通路用于修复高复制压力和氧化压力导致的大量DNA损伤。但是,由于相关动物模型的缺乏,科学家们尚无法判断体内环境下包括肝细胞癌在内的多种肿瘤发生与发展过程中DSB修复能力的变化情况,因此也很难评估是否可通过靶向DNA损伤修复以治疗肝细胞癌及其它类型肿瘤。
研究团队将基于绿色荧光蛋白 GFP 建立的检测HR的报告载体整合到小鼠基因组Rosa26位点(图1),建立了体内检测HR效率的报告小鼠模型,同时结合Gorbunova教授课题组赠予的NHEJ报告小鼠模型,通过尾静脉注射将外源 I-SceI质粒导入小鼠肝脏,从而诱导报告载体发生定点的DSB。若细胞成功通过 HR 或者NHEJ 修复该损伤,细胞会发出绿色荧光,因此可以定量分析组织中HR 或 NHEJ 修复的频率。在 DEN/CCl4/乙醇诱导的小鼠肝细胞癌模型中检测发现,相比于癌旁组织,HR 和 NHEJ 在癌组织中分别提升了1.6和2.5倍。
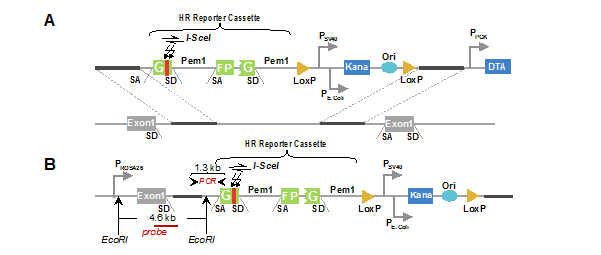
图1 HR检测报告载体
为探究 HR 和 NHEJ 在癌组织中提升的原因,研究团队检测了小鼠癌组织及癌旁组织中DSB修复通路中各蛋白的表达情况,发现关键修复因子PARP1 和 DNA-PKcs 的表达显著提升。而团队成员利用大量临床标本进一步验证发现,上述两种蛋白在人类肝细胞癌中依然呈现明显的表达上调,暗示其在DSB修复的激活和肝细胞癌发展维持中扮演了重要角色。进一步研究显示,利用PARP1 抑制剂olaparib 和 DNA-PKcs 抑制剂NU7441同时处理肝细胞癌细胞可以极大地抑制其 HR 和 NHEJ 修复能力。更为重要的是,联合应用olaparib 和NU7441,或同时敲降 PARP1和DNA-PKcs都可协同抑制肝细胞癌细胞的增殖,证明二者可作为治疗肝细胞癌的潜在靶标。后续的机制研究发现,olaparib 可通过抑制 PARP1酶活,从而阻碍 ALC1 在损伤位点的募集,继而延缓损伤位点周围核小体的清除,最终抑制 RPA2 和 RAD51 在损伤位点的招募。最后,研究团队基于小鼠原位肝细胞癌和人肝细胞癌PDX模型,进一步证实了olaparib 和 NU7441 联用通过靶向DSB修复以治疗肝细胞癌的巨大潜力(图2)。

图2 Olaparib和NU7441联合疗法高效抑制肝细胞癌
研究团队建立了体内检测肝细胞DSB修复效率的新方法。本项研究中建立的小鼠模型有助于肿瘤、衰老以及其它研究领域深入探索体内环境下DSB变化及其调控机制。该工作还发现了导致HCC中DSB能力提升的关键基因 PARP1 和 DNA-PKcs,并阐明了肝细胞癌中PARP1 调控HR 的机制。本项研究中olaparib 和 NU7441联合疗法的成功临床前应用提示,靶向DSB修复在肝细胞癌治疗中具有潜在的临床应用价值。此外,该研究也拓宽了 PARP1 抑制剂在肿瘤治疗中的应用,也为肝细胞癌的后续治疗提供了重要的理论基础。
同济大学生命科学与技术学院博士后研究人员王晨、博士研究生唐欢胤、附属第一妇婴保健院助理研究员耿安珂、东方肝胆外科医院医生戴炳华为本文的共同第一作者。毛志勇教授、孙方霖教授和蒋颖副教授为本文的共同通讯作者。该研究成果得到国家重点研发计划、国家自然科学基金、上海市优秀学术带头人计划、上海市教委与上海市教育发展基金会“曙光”计划等项目资助。
原文链接:https://www.pnas.org/content/early/2020/10/02/2002917117
